- Accueil
- Publications
- Les interventions de cardiologie et l‘environnement interventionnel
- Les interventions
- L'électrophysiologie cardiaque et l'ablation
- L'ablation de tachycardie ventriculaire
L'ablation de tachycardie ventriculaire
Bérénice LANAU-PAILLÉ, infirmière en rythmologie, Clinique Ambroise Paré, Neuilly sur Seine,
Décembre 2023
La tachycardie ventriculaire (TV) est un trouble du rythme cardiaque qui prend naissance dans les ventricules. Sa fréquence est supérieure ou égale à 120 battements par minutes (bpm) (voire supérieure à 100 bpm) avec une dissociation de l’activité électrique des oreillettes et des ventricules. Elle correspond, par définition, à plus de trois extrasystoles ventriculaires (ESV) à la suite les unes des autres avec des complexes QRS caractéristiques sur l’électrocardiogramme (ECG), d’une largeur supérieure ou égale à 120 millisecondes (ms) voire même supérieur à 200 ms dans le cas d’une TV épicardique. La morphologie des QRS, dépolarisation électrique des cellules ventriculaires, sur les dérivations de l’ECG permet de prédire l’origine de la tachycardie. Par définition, une TV est considérée comme stable et monomorphe contrairement à la fibrillation ventriculaire (FV) qui est instable et polymorphe. En tachycardie ventriculaire, l’onde P n’est pas toujours visible sur l’ECG.
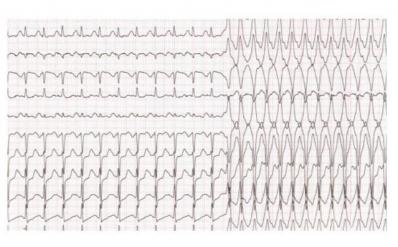
1- GENERALITES ET DEFINITIONS
1/ A Prévalence
90% des TV sont associées à une cardiopathie déjà existante, à savoir la cardiomyopathie ischémique (CMI), la dysplasie arythmogène du ventricule droit (DVDA), la cardiomyopathie dilatée (CMD), la cardiomyopathie hypertrophique (CMH), … Ces cardiopathies créent des zones de de fibrose et donc de cicatrice (endocavitaires et/ou épicardiques) au niveau du myocarde provoquant généralement la formation d’un mécanisme de réentrée de l’influx électrique avec des isthmes critiques à l’origine des tachycardies ventriculaires.
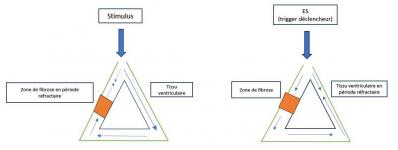
Figure 2: Mécanisme électrophysiologique de réentrée
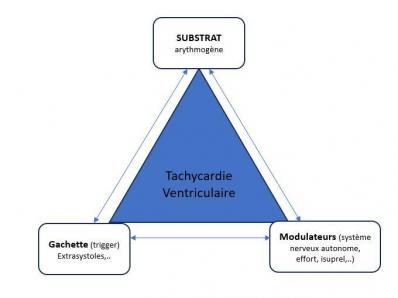 Figure 3 : Triangle du Ph Coumel 1987, rappels des facteurs nécessaires à l’arythmogénèse
Figure 3 : Triangle du Ph Coumel 1987, rappels des facteurs nécessaires à l’arythmogénèse
10% des TV se déclenchent sur un cœur sain. Ce sont des TV où il n’y a pas de zone cicatricielle. On parle de TV idiopathiques. Certaines sont bénignes comme la TV infundibulaire qui est la plus fréquente ou la TV fasciculaire. D’autres résultent de facteurs génétiques préexistants (comme le syndrome du QT long, le syndrome de Brugada, les tachycardies polymorphes catécholergiques (TVPC)) ...
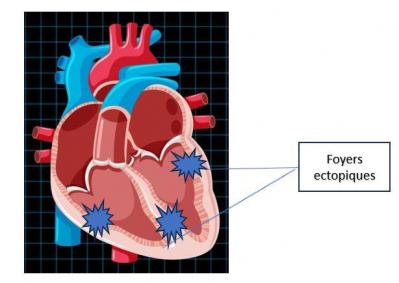
Figure 4: Foyers ectopiques de TV sur cœur sain
Exemples de cardiopathies cardiaques associées et définitions :
◦ CMI : les Cardiomyopathies Ischémiques sont des maladies coronariennes consécutives à un défaut d’apports en oxygène du muscle cardiaque en raison de l’obstruction partielle ou complète d’une ou plusieurs des artères coronaires entourant le cœur. L’appauvrissement des tissus en oxygène provoque la création de lésions au niveau du myocarde et donc une ischémie (transitoire ou non) pouvant aller jusqu’à la nécrose du tissu myocardique.
◦ DVDA : la Dysplasie Arythmogène du Ventricule Droit est une maladie du muscle du cœur dans laquelle les cellules musculaires cardiaques sont progressivement remplacées par du tissu adipeux et du tissu fibreux (fibrose) créant ainsi des zones cicatricielles. Les cicatrices sont susceptibles ensuite de participer à la formation d’arythmies et de favoriser la dysfonction ventriculaire.
◦ CMH : la Cardiomyopathie Hypertrophique est une maladie portant atteinte à la structure cellulaire du ventricule gauche. On parle d’hypertrophie cellulaire. Le tissu cardiaque s’épaissi jusqu’à la formation de plages de fibroses arythmogènes.
◦ CMD : la Cardiomyopathie Dilatée correspond à la dilatation des parois du ventricules (surtout du ventricule gauche) induisant une diminution de la contraction du muscle cardiaque et donc une diminution de la fraction d’éjection ventriculaire (FeVG).
Exemples de cardiopathies génétiques et définitions :
◦ Syndrome du QT long : Le Syndrome du QT long est une maladie génétique qui se caractérise par des anomalies électriques sur l’électrocardiogramme ainsi que par un risque d’arythmie ventriculaire, de syncope et d’arrêt cardiaque. La structure et le fonctionnement du muscle cardiaque sont normaux.
◦ Syndrome de Brugada : Il s’agit d’une maladie génétique responsable de troubles du rythme ventriculaires, décrite en 1992 par les frères Brugada. Elle est à risque de syncope voire de mort subite sur un cœur sain. Un test à l’Ajmaline® (ou parfois Flécaine®) est réalisé en salle d’électrophysiologie en cas de suspicion. Si le test est positif avec des modifications caractéristiques de l’ECG, les patients à haut risque rythmique (syncope par exemple) sont ensuite appareillés avec un défibrillateur en prévention primaire de la mort subite.
1/B Les facteurs de risques
Une cicatrice d’infarctus et/ou une maladie du myocarde ventriculaire augmentent donc le risque de développer des tachycardies ventriculaires. De même un individu n’ayant aucun antécédant de cardiopathies sous-jacentes mais où l’on recense dans les antécédents familiaux des maladies génétiques pouvant être associées à des déclenchements de tachycardie ventriculaire, ou même des morts subites, sont des personnes à risque de présenter ce type d’arythmie.
1/C Symptômes de la TV ventriculaire chez le patient
Les épisodes de tachycardie ventriculaires sont variables d’un individu à l’autre. Ils peuvent être de courte durée (quelques secondes) et bien tolérés, le patient est dit asymptomatique. Mais ils ont la possibilité d’être soutenus et symptomatiques : le patient ressent des palpitations souvent associées à une dyspnée, parfois des douleurs thoraciques rétrosternales, voire des vertiges si la tachycardie est très rapide et mal tolérée pouvant conduire à une syncope. La tachycardie ventriculaire est également susceptible de se dégrader en fibrillation ventriculaire (tachycardie ventriculaire instable, anarchique et polymorphe).
1/D Anatomie
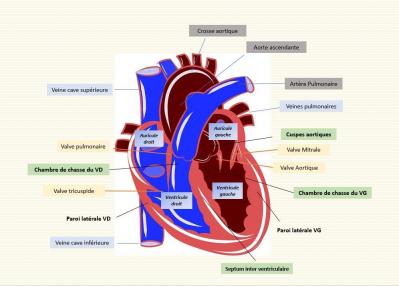
Figure 5 : Anatomie du cœur
Rappels de la localisation des structures anatomiques d’intérêt dans l’ablation des tachycardies ventriculaires :
- Right ventricular outflow tract (RVOT) la chambre de chasse du VD (à l’entrée de l’artère pulmonaire)
- Left ventricular outflow tract (LVOT) la chambre de chasse du VG (vestibule aortique)
- Cuspes aortiques : naissance des artères coronaires sur deux des trois cuspes, la troisième est dite non coronaire.
- Les piliers : cônes musculaires où s’insèrent le cordage des valves mitrale et tricuspide
- Infundibulum : partie de la chambre de chasse du ventricule droit située immédiatement sous l’orifice valvulaire pulmonaire.
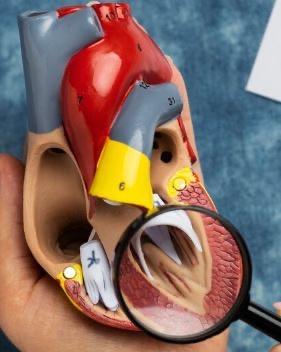
Figure 6: Valves et cordages
1/E Localisation des tachycardies ventriculaires en analysant l’électrocardiogramme 12 dérivations
La localisation de la TV s’établie (comme pour celle des ESV) selon quatre étapes grâce à l’interprétation de la morphologie du complexe QRS sur les différentes dérivations frontales et transversales de l’électrocardiogramme 12 D.
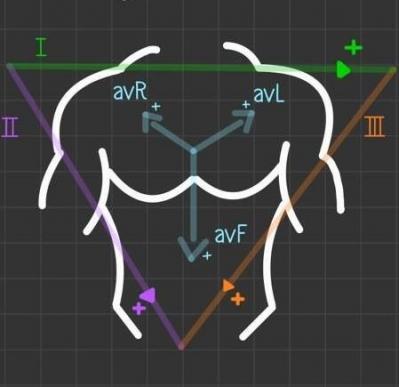
Figure 7 : Triangle de Willem Einthoven
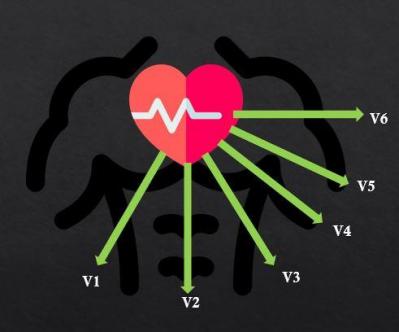
Figure 8 : Dérivations précordiales, coupe transversale
-
La dérivation précordiale V1 (4ème espace intercostal droit près du sternum) renseigne sur le ventricule concerné.
Si V1 NEGATIF : la TV provient du ventricule droit avec aspect d’un bloc de branche gauche.
Si V1 POSITIF : la TV a pour origine le ventricule gauche avec aspect d’un bloc de branche droit.
-
Analyse des dérivations inférieures D2, D3 et AVF
Si NEGATIVES : axe supérieur correspondant à la région inférieure du ventricule
Si POSITIVES : axe inférieur correspondant à la région supérieure du ventricule.
-
D1 et VF
Axe Gauche : le QRS est POSITIF en D1 et négatif en aVF, dans le VD l’origine sera latérale ou dans le VG elle sera septale
Axe Droit : le QRS est NEGATIF en D1 et positif en aVF, dans le VD l’origine sera septale ou dans le VG elle sera latérale.
-
Comparaison des précordiales de V1 à V6 selon la transition (= passage de l’aspect rS à l’aspect Rs ou aspect R sur S =1)
Transition en v1 et v2 : paroi du VD et septum interventriculaire (partie haute)
Transition v3 et v4 : partie antérieure du septum interventriculaire et apex du VG
Transition v5 et v6 : partie antérieure moyenne de la paroi libre du VG
1/F Critères d’ablation
Il existe plusieurs critères d’ablation comme la récidive d’une TV sous traitement médicamenteux optimal, la présence de chocs répétitifs par un patient porteur d’un défibrillateur… L’ablation est proposée pour améliorer la qualité de vie du patient et non son espérance de vie.
2- PROCEDURE D’ABLATION D’UNE TACHYCARDIE VENTRICULAIRE
L’ablation de TV a pour objectif de détruire les zones du myocarde responsables de l’induction de la tachycardie ventriculaire, par radiofréquence (une énergie thermique délivrée par un cathéter d’ablation) à l’aide d’un système de cartographie 3D. Plusieurs acteurs essentiels sont idéalement présents (tous les centres ne bénéficient pas d’un médecin anesthésiste-réanimateur ni d’IADE pour toutes leurs procédures en salle de cathétérisme) pour le bon déroulement de l’intervention : le médecin anesthésiste présent sur le plateau technique, l’infirmier anesthésiste en charge de la sédation et du confort du patient, le médecin rythmologue procédant à l’ablation, l’infirmier de salle de rythmologie et l’ingénieur d’application du système de cartographie utilisé par le centre.
2/A Pré requis pour le patient
Le patient doit être à jeun stricte depuis 6 heures, bénéficier d’un bilan sanguin complet avec une carte de groupe sanguin et RAI, avoir signé un consentement opératoire, obtenu une consultation d’anesthésie en amont et être suffisamment stable sur le plan médical pour supporter la procédure d’ablation susceptible de durer dans le temps, parfois 3 heures voire plus selon sa complexité. Au préalable, le patient présente un rasage au niveau du thorax et du short afin de bénéficier d’une asepsie optimale et de favoriser l’adhérence des différentes électrodes et plaques nécessaires à l’intervention (notamment en cas de cardioversion en urgence) ainsi que celle des pansements compressifs réalisés au niveau des points de ponction en fin de procédure. Il doit également réaliser une douche avec un savon antiseptique type Bétadine© ou Hibiscrub© avant son entrée en tenue de bloc opératoire en salle de cathétérisme.
Des examens préopératoires sont en général prescrits en amont par le cardiologue, à savoir :
- Un électrocardiogramme
- Une échographie transthoracique : ETT, qui est un examen d’imagerie utilisant les ultrasons permettant de visualiser et mesurer les flux entre les différentes cavités cardiaques ainsi que de mesurer la taille de ces cavités et la fraction d’éjection du ventriculaire gauche.
- Un scanner cardiaque avec injection d’iode qui permet de visualiser la morphologie de toutes les structures cardiaques, artères coronaires, piliers, … ainsi que d’éliminer ou non la présence de thrombus intra cavitaire (qui serait une contre-indication à l’ablation)
- Un bilan sanguin complet

Figure 9: Dossier patient pré opératoire
2/B Rôle de l’IDE en salle d’intervention et installation du patient
L’infirmier en salle de rythmologie joue un rôle primordial. Il est avant tout responsable de la mise en route de la salle et en assure l’ouverture journalière. Il en contrôle le bon fonctionnement et réalise les branchements de tous les dispositifs et interfaces présents (baie d’électrophysiologie, générateurs, stimulateur externe, scopie, systèmes de cartographie 3D, présence du matériel nécessaire à l’ablation…). Il vérifie également la présence et la bonne activité des équipements susceptibles d’être mis en œuvre en cas d’urgence à savoir le défibrillateur, le système d’aspiration, la présence d’un pacemaker externe fonctionnel, l’oxygène mural, … Tout ceci est consigné sur la feuille de traçabilité d’ouverture de salle. L’IDE accueille le patient pour son ablation de tachycardie ventriculaire conjointement avec l’infirmier anesthésiste. Ensemble, ils vérifient le dossier pré opératoire qui doit être complet (bilan sanguin, consultation d’anesthésie, désignation de la personne de confiance (loi n° 2002-303 du 4 mars 2002 du Code de la Santé Publique et relative « aux droits des malades et à la qualité de vie du système de Santé »), examens pré opératoires prescrits réalisés, consentement opératoire daté et signé, …). L’infirmier de salle procède à la vérification croisée de lacheck-list préopératoire avec l’IADE et le médecin anesthésiste en appliquant les règles d’identitovigilance requises. Ils installent confortablement le patient, préalablement perfusé, en décubitus dorsal sur la table d’intervention et mettent en place la surveillance clinique sous scope en lui fournissant toutes les explications nécessaires et en répondant à ses questions. Les patchs de défibrillation sont positionnés de manière antéro-latérale et banchés au défibrillateur de la salle prêt à l’emploi. L’infirmier met en place l’ECG 12 dérivations de la baie d’électrophysiologie, s’assure avec l’ingénieur d’application des bons branchements des câbles du système de cartographie et de la baie, ainsi que du positionnement correct des patchs du système de cartographie 3D. Les membres supérieurs voire également inférieurs du patient sont contentionnés pour éviter tout contact avec les champs opératoires et le matériel stérile. L’infirmier de salle vérifie la bonne compréhension du patient concernant le déroulement de la procédure et des suites post opératoires, le rassure si nécessaire. Il s’assure également d’avoir bien rentré l’identité complète du patient sur les dispositifs médicaux essentiels à l’intervention à savoir la scopie, la baie d’électrophysiologie et le système de cartographie.
Si le patient est porteur d’un défibrillateur celui-ci doit être désactivé par le médecin à l’aide du programmateur dédié afin d’inhiber la délivrance des thérapies (chocs, stimulation anti tachycardique ATP « Anti Tachycardia Pacing »). Il sera reparamétré en fin de procédure par le cardiologue.
Le logiciel d’enregistrement des données de l’intervention de l’établissement (MediReport© par exemple) doit être à jour et complété par l’infirmier de salle pour assurer la rédaction des documents de traçabilité et transmettre les observations afin de garantir la bonne continuité des soins.
Enfin l’infirmier de salle prépare une table stérile, et tout le matériel nécessaire à l’ablation de tachycardie ventriculaire.
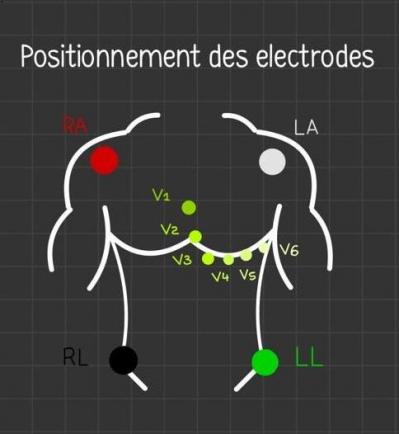
Figure 10: Positionnement des électrodes du système de cartographie
2 / C Anesthésie et voies d’abord
La procédure d’ablation de tachycardie ventriculaire s’effectue dans la majorité des cas sous sédation (légère puis renforcée au moment des tirs de radiofréquence) ou alors parfois, dans des cas bien spécifiques, sous anesthésie générale comme pour les abords épicardiques. En effet les médicaments d’anesthésie générale sont susceptibles d’empêcher le déclenchement des tachycardies ventriculaires qui ne sont alors plus inductibles. Selon les habitudes du centre, le rythmologue introduit plusieurs cathéters par voie veineuse fémorale sous anesthésie locale à l’aide de désilets : la sonde du sinus coronaire (décapolaire), une sonde d’ablation et un cathéter de mapping multi électrodes.
Si la tachycardie se trouve dans le ventricule gauche le praticien a la possibilité d’accéder aux cavités gauches du cœur, selon la localisation de la TV, par :
- voie transeptale en effectuant une ponction du septum interauriculaire sous scopie à l’aide d’une pression artérielle intra cavitaire en temps réelle et également sous contrôle de l’échographie transoesophagienne (ETO) ou encore de l’échographie intracardiaque
- voie rétro aortique (en franchissant la valve aortique) en ponctionnant l’artère fémorale comme voie d’abord. On utilisera un système de fermeture artériel en fin d’intervention de type Femoseal® ou Angioseal®.
A noter que l’administration d’héparine intraveineuse est nécessaire en cas d’intervention à gauche afin de diminuer le risque d’événements thromboemboliques indésirables. Le TCA « temps de céphaline avec activateur », indique le temps de la coagulation du sang en millisecondes. Il est mesuré tout au long de l’intervention (selon un protocole médical établi) si celle-ci a lieu dans les cavités gauche du cœur, par l’infirmier de salle ou l’IADE. Le bolus d’héparine initial post transeptale, ou ponction rétro aortique, peut être complété si besoin à la demande du médecin si le TCA n’est pas optimal, c’est-à-dire s’il n’est pas supérieur à 300ms.
Dans certains cas l’origine de la TV est épicardique, l’opérateur effectue alors une ponction péricardique sous xiphoïdienne (sous anesthésie générale) sous scopie (risques d’hémorragie péricardique accrus, sténose des coronaires, choc cardiogénique, …).
2/D La procédure d’ablation de tachycardie ventriculaire en cartographie
Elle se scinde en deux grandes parties : une première phase dite diagnostique afin d’identifier l’origine de la TV clinique grâce à un système de cartographie 3D et une seconde phase d’ablation où le rythmologue va aller cautériser la zone cellulaire responsable de la tachycardie par radiofréquence.
2/D.1 Cartographie 3D

Figure 11: Exemples de systèmes de cartographie 3D
Pour cette première étape de cartographie l’opérateur utilise soit un cathéter de mapping multi électrodes tel que le Pentaray®, l’Octaray®, l’Orion®, le HD Grid® … ou alors un cathéter monosonde d’ablation de type SmarttouchSF®, Qdot®, Intellanav®, Tactiflex®, ... selon le système de cartographie utilisé.
Dans un premier temps, si le patient n’est pas en TV, l’ingénieur d’application va réaliser une carte de voltage bipolaire en rythme sinusal. Cette carte permet d’analyser l’amplitude des signaux électriques endocavitaires recueillis entre deux électrodes par la sonde de mapping. L’échelle d’amplitude définit pour le ventricule est de 0.5mV à 1.5mV. Si le tissu est sain le signal recueilli sera matérialisé par la couleur rose correspondant aux valeurs les plus hautes de l’échelle d’amplitude du signal électrique en millivolts ; à l’inverse, plus le tissu sera nécrosé et donc bas volté plus il tendra vers la couleur rouge sur la carte de voltage (<0.5mV). A noter que par définition pour les TV idiopathiques la carte de voltage ne présente pas de zones dites « bas voltées » car il n’y a pas de zone cicatricielle, le cœur du patient est sain. A contrario, en ce qui concerne les TV avec cardiopathie associée, il s’agit pour le cardiologue d’identifier la zone de cicatrice, donc de substrat, bas voltée engendrée par la maladie. Soulignons également qu’il est possible de ne pas retrouver de zones cicatricielles pour une TV sur cardiopathie et qu’il faille alors aller voir en épicardique c’est-à-dire à la surface du cœur et non plus dans les cavités cardiaques pour réaliser la carte de voltage et trouver une zone cicatricielle. Le patient est également susceptible de présenter une cicatrice à la fois endocavitaire et épicardique révélant des circuits de macro-réentrées complexes. Pendant la cartographie l’ingénieur d’application repèrera avec le médecin et l’infirmier de salle les signaux endocavitaires correspondants aux voies de conductions physiologiques (tissu nodal) afin de les matérialiser géographiquement sur la carte (à savoir le faisceau de His, réseau de Purkinje, les branches, ...).
L’ingénieur d’application a la possibilité de convertir la carte de voltage en carte d’activation pour visualiser la propagation de l’influx électrique cardiaque en rythme sinusal dans le temps et de repérer puis marquer les potentiels tardifs appelés « LAVA » (Local Abnormal Ventricular Activity) pour les TV sur cardiopathie cardiaque. Ces signaux sont caractéristiques des potentiels électriques lents situés au niveau des isthmes critiques des macro-réentrées dues aux zones cicatricielles. Ils sont souvent de faible amplitude et très tardifs, à ne pas confondre avec le « far-field » du ventricule. On recherche les LAVA tardifs (après le QRS) les plus précoces. Ils sont situés à l’entrée de la voie lente de l’isthme critique.
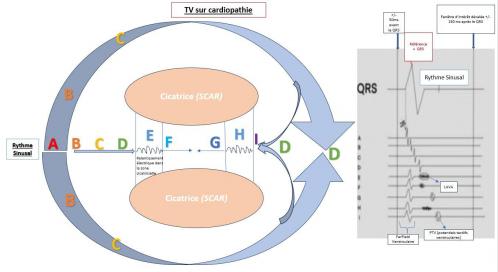
Figure 12: Cartographie en rythme sinusal TV avec substrat, signaux caractéristiques
Une fois que le tissu ventriculaire est analysé en rythme sinusal on essaie de déclencher la tachycardie ventriculaire. Pour cela plusieurs prérequis sont nécessaires : éviter les médicaments d’anesthésie générale qui masquent la TV et surtout s’assurer que le patient tolère bien la tachycardie ventriculaire. L’IADE et l’anesthésiste sont prêts à intervenir si le patient n’est pas stable hémodynamiquement en TV et syncope. De même l’IDE de salle est opérationnel pour « over-driver » la TV avec le stimulateur externe de la baie de KT (c’est-à-dire à stimuler 20 ms en dessous du cycle de la tachycardie ventriculaire pour la « casser ») et/ou à aller choquer le patient sur décision des médecins si besoin. Pour déclencher la TV on réalise une stimulation ventriculaire programmée (SVP) grâce au stimulateur externe de la baie d’électrophysiologie. L’IDE va stimuler le ventricule du patient (le médecin place une sonde dans le ventricule d’intérêt) avec un train fixe et une extrasystole décrémentielle jusqu’au déclenchement de la TV ou jusqu’à avoir atteint la période réfractaire (PRE) du ventricule. Si la TV ne se déclenche pas on ajoute une deuxième extrasystole décrémentielle au protocole de SVP en gardant un train fixe et une première extrasystole fixe légèrement supérieure à la PRE du ventricule trouvée précédemment (environ 10 ms). Le protocole continue ainsi jusqu’à 3 extrasystoles programmées si le patient le supporte bien hémodynamiquement et ce jusqu’au déclenchement de la TV. L’IADE peut être amené à réaliser une perfusion d’Isuprel® à la demande du médecin pendant la SVP afin de favoriser le déclenchement de la TV. L’isoprénaline est un médicament agoniste de la famille des récepteurs adrénergiques. On l’utilise en électrophysiologie pour reproduire l’activité électrique du cœur à l’effort. Notons qu’il est primordial de bien mémoriser le couplage d’extrasystoles permettant de provoquer la tachycardie ventriculaire sur la baie de KT afin de le reproduire en fin de procédure et ainsi valider le succès de l’ablation.
Au démarrage de la TV l’ingénieur d’application réalise rapidement une carte d’activation afin de « mapper » le circuit de la tachycardie et donc le mécanisme de réentrée pour une TV sur cardiopathie sous-jacente. Pour une TV idiopathique il s’agira de trouver le foyer ectopique de cellules électriques qui déchargent.
L’activation de la TV va se matérialiser de différentes couleurs selon une fenêtre prédéfinit : (le cycle de la TV en ms – 10)/2. La fenêtre d’intérêt est paramétrée automatiquement sur le QRS qui sert de référence. Pour une TV avec réentrée on cherchera les potentiels « mid-diastoliques » caractéristiques des zones de conduction lente. Le circuit de la tachycardie sera matérialisé sur la carte selon des couleurs prédéfinies. (cf figure14)
Certains centres réalisent également des cartes d’activation complexes en DEEP Mapping (Decrement Evoked Potential) en TV avec une extrasystole décrémentielle.
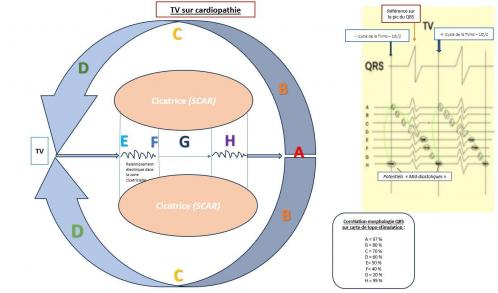
Figure 13: signaux caractéristiques carte d'activation en TV avec substrat
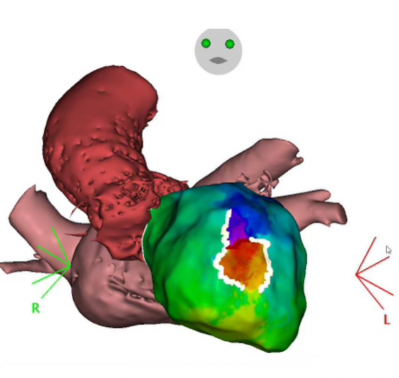
Figure 14: Système de cartographie Biosense Webster, carte d’activation d’une TV endocardique sur cardiopathie associée, Professeur Raphaël Martins CHU de Rennes
Si malgré la stimulation ventriculaire programmée et l’administration d’Isoprénaline intra veineuse la TV n’est pas déclenchable, l’ingénieur d’application proposera au rythmologue de réaliser une carte de « pace mapping » c’est-à-dire de topo stimulation. Il s’agit d’aller stimuler différentes parties du ventricule d’intérêt et de comparer les QRS stimulés (et non les QRS mécaniques c’est-à-dire ceux liés aux mouvements du cathéter) avec celui de la TV clinique de référence dont on a pris le « pattern », (c’est à dire la morphologie) au préalable. Les meilleures corrélations sont matérialisées d’une certaine couleur et doivent normalement se trouver au niveau du point de sortie de la TV et donc de la zone à ablater (cf figure 14).
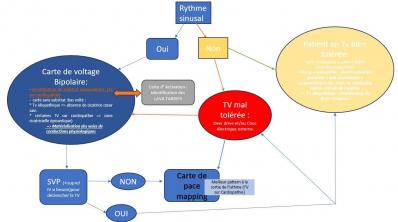
Figure 15: Workflow, résumé
2/D.2 Ablation
Une fois que l’origine du foyer de la TV idiopathique ou que l’isthme critique du circuit de la TV sur cardiopathie a été identifié le rythmologue va procéder à l’ablation par radiofréquence. Pour cela il utilise un cathéter d’ablation monosonde de type SmarttouchSF®, Qdot®, Intellanav®, Tactiflex®...selon le système de cartographie utilisé. Dans le cas d’une tachycardie ventriculaire sur cœur sain il est essentiel d’avoir pu déclencher la TV afin d’identifier le foyer ectopique sinon il est impossible de cartographier quelque chose et donc de procéder à l’ablation. Car rappelons-le encore une fois ici il s’agit d’une tachycardie sur un cœur sain sans zone de cicatrice et donc sans substrat cartographiable. Dans le cas d’une TV sur cardiopathie sous-jacente il y a plusieurs cas de figures selon si on a réussi à déclencher la tachycardie ou non. Le médecin ablate les potentiels tardifs LAVA identifiés en rythme sinusal lors de la carte du substrat. Ou alors la TV a été déclenchée grâce à la stimulation ventriculaire programmée et ainsi cartographiée. Le médecin ablate alors l’isthme critique identifié où le courant électrique se déplace plus lentement entre les zones cicatricielles. Les tirs d’ablation en radiofréquence dans le ventricule se situent généralement entre 30-45 Watts suivant la région d’intérêt. Selon la zone d’ablation retenue, il est important de situer les artères coronaires qui irriguent le cœur et plus encore si l’ablation a lieu en épicardique. Si un scanner a été réalisé en amont et segmenté, il est associé et recalé sur la cartographie pour localiser précisément les coronaires. Si ce n’est pas le cas, il est essentiel qu’un cardiologue interventionnel réalise une coronarographie avant l’ablation pour visualiser précisément la géographie des artères coronaires en scopie par rapport à la zone d’ablation privilégiée. En effet il existe un risque important de sténose d’une coronaire si elle est située à proximité de l’endroit à ablater en radiofréquence. Après l’ablation plusieurs critères viennent valider le succès de la procédure :
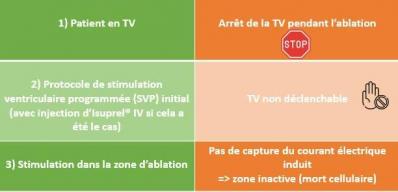
Tableau 1: Critères de succès d'ablation
Si ce n’est pas le cas, l’équipe recommence à cartographier la TV si elle reste déclenchable car les tirs d’ablations modifient la structure de l’isthme critique. Cette intervention est susceptible de durer plusieurs heures car contrairement aux oreillettes, le tissu ventriculaire est épais donc plus difficile à ablater et certaines zones anatomiques sont difficiles d’accès (piliers, cuspes, …) le cathéter d’ablation est alors susceptible de manquer de stabilité et l’opérateur peut avoir recours à une gaine déflectable de type Agilis®, Vizigo®, ...
2/D.3 Post intervention
En fin de procédure, après un dernier ACT de contrôle pouvant donner lieu à l’injection de protamine (antidote de l’héparine) s’il est considéré comme trop élevé par le médecin ; un pansement compressif est réalisé par l’infirmier au niveau des points de ponctions. L’opérateur a recours à un système de fermeture artériel type Angioseal® ou Femoseal® s’il a ponctionné l’artère fémorale pour passer en rétro aortique. Les consignes sont à nouveau transmises au patient, il doit rester allonger durant 6 heures post intervention (inclinaison du buste à 30-40 degrés maximum) afin d’éviter tout saignement au niveau des points de ponction et donc la formation d’un éventuel hématome. L’équipe réalise le bilan des apports de solutés au patient (côté anesthésie et rythmologie) sur la totalité de la procédure, les sondes étant irriguées pour certaines et la procédure pouvant durer plusieurs heures... Les informations sont transmises à l’opérateur qui prescrira ou non des diurétiques au patient en post intervention. Si le patient est porteur d’un défibrillateur, il doit être contrôlé et réactivé par le rythmologue. Le médecin réalise une échographie cardiaque post intervention afin de visualiser un éventuel épanchement péricardique et le patient est conduit sous scope en salle de réveil (SSPI) où il sera à nouveau monitoré et surveillé hémodynamiquement et cliniquement avant de retourner en chambre.
Conclusion
L’ablation de tachycardie ventriculaire est une procédure complexe nécessitant un support cartographique et tout une équipe coordonnée autour du patient dans un centre de mention C. Elle est susceptible de durer parfois plusieurs heures. Au travers de cet article nous avons tenté de définir la tachycardie ventriculaire, de rappeler ses mécanismes, ses localisations, et de présenter le déroulement d’une procédure d’ablation comme nous l’effectuons en salle de cathétérisme cardiaque à la clinique Ambroise Paré de Neuilly sur Seine.
Références :
- « Conduite à tenir devant un électrocardiogramme » 147 théraplix, problèmes médicaux quotidiens
- « Lumières sur la rythmologie » Cordiam impact médicom
- https://www.icm-mhi.org : Institut de cardiologie de Montréal
- https://programme.europa-organisation.com
- International Virtual EP Talk, Youtube Channel
- Carto NURSE meeting Biosense Webster, formation TV/ESV